iGEM – DTU 2022
Du har helt sikkert hørt om nogle af de miljømæssige problemer, verden står overfor. Du har sikkert også hørt, at afbrænding af fossile brændstoffer bærer en del af skylden for de klimaforandringer, verden oplever. Mange arbejder på at løse disse problemer f.eks. ved at skabe bæredygtige alternativer til fossile brændstoffer. Disse alternativer kommer f.eks. fra land- og skovbrug, men produktionen af biobrændstof er blevet kritiseret for ikke at skabe nok værdi for samfundet, da energikilderne ofte ender med at konkurrere med fødevareproduktionen for råstoffer.
Den bioøkonomiske værdipyramide
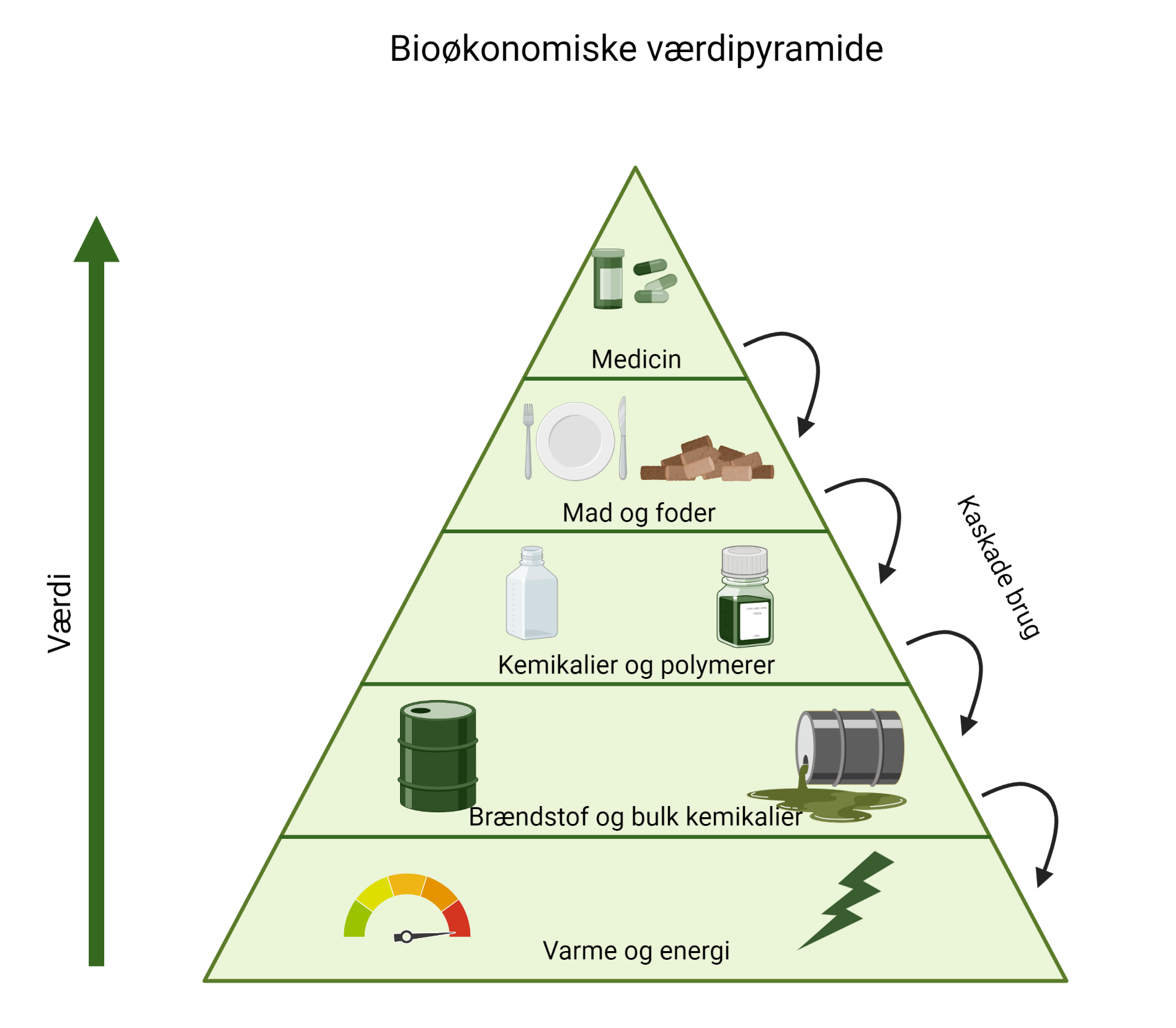
Nu tænker du måske; “Brændstof har da også værdi!”, og du har helt ret. Men når biomasse bliver brugt til at producere varme og energi, kan det ikke senere blive brugt til at producere andre produkter. Værdien af produkter skabt fra biomasse er illustreret i den bioøkonomiske værdipyramide, som du kan se i figur 1.
Den bioøkonomiske værdipyramide beskriver, hvordan brugen af biomasse bør prioriteres. Øverst i den bioøkonomiske værdipyramide ses medicin og andre meget dyrebare kemikalier (f.eks. komplekse enzymer), herefter kommer mad til os og foder til vores dyr, efterfulgt af forskellige kemikalier og polymerer, så som bioplastik. Længere nede i den bioøkonomiske værdipyramide ses brændstof og simple kemikalier som vi producerer i store mængder (det kalder vi bulk kemikalier), og nederst i pyramiden, med den laveste værdi pr. masseenhed, ses varme og energi.
En smart måde at bruge biomasse på er at lade biomassen falde som vand i et vandfald ned igennem den bioøkonomiske værdipyramide. Med andre ord kan man bruge overskydende biomasse fra produktion af medicin til produktion af foder, mens overskydende biomasse fra produktion af foder kan bruges til produktion af bioplastik. Denne vandfaldseffekt kalder vi kaskadeanvendelse.
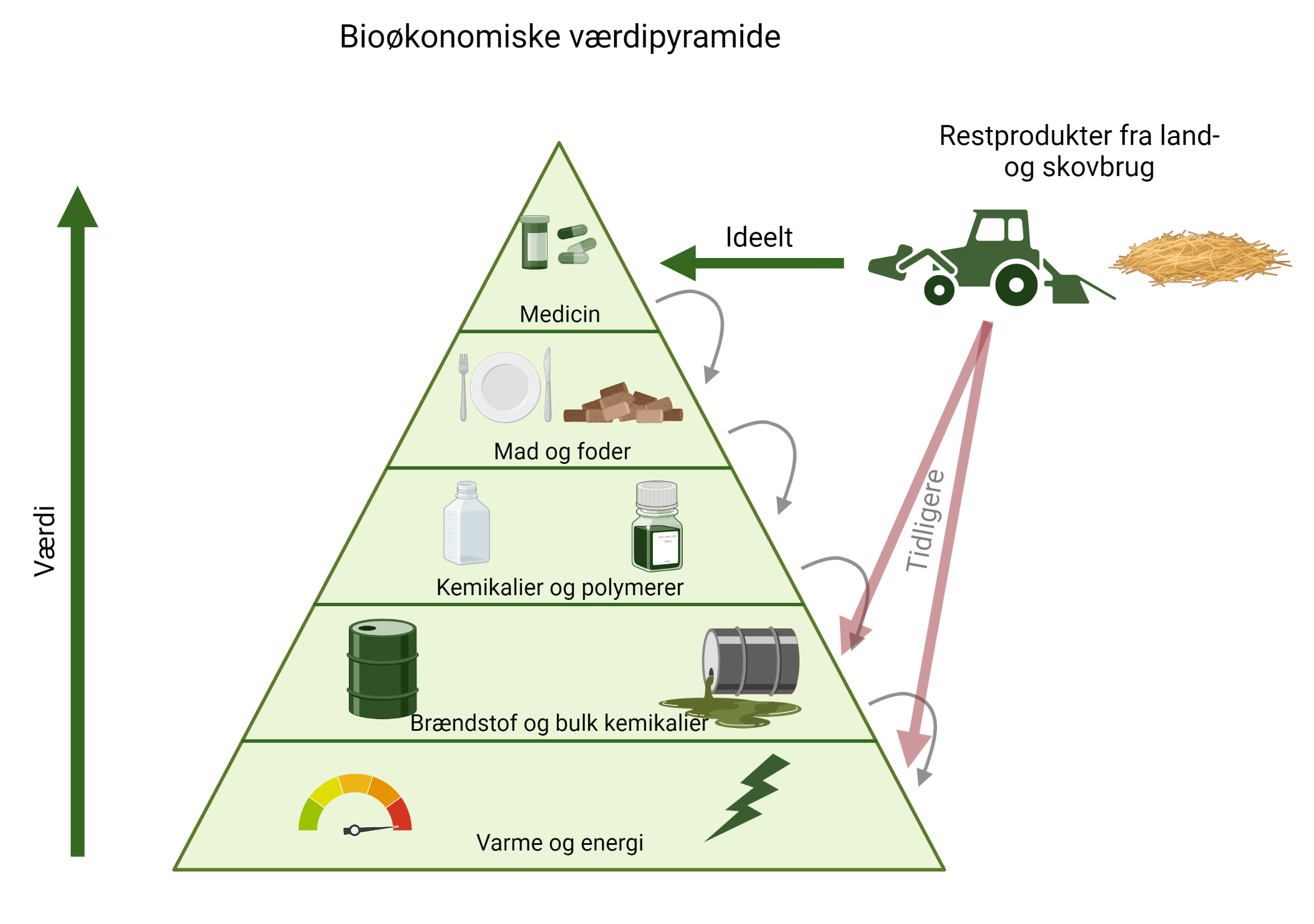
Som du kan høre, er det altså ikke optimalt, at restprodukter fra land- og skovbrug bliver brugt til at skabe varme og energi med det samme. I stedet bør vi forsøge at bruge restprodukterne til at lave produkter med en høj værdi, eksempelvis medicin. Restprodukterne kan løbe ned igennem den bioøkonomiske værdipyramide vha. kaskadeanvendelse, for til allersidst at blive brugt til at skabe varme og energi. Dette kan du også se i figur 2.
Hvorfor bruger vi ikke restprodukter til produktion af medicin?
Før du læser videre, kan du prøve at gætte selv; Kan du komme med forslag til, hvorfor vi ikke gør brug af denne energikilde til produktion af højværdi produkter?
For at kunne frigive energikilder (oftest sukre) i biomassen, som cellefabrikker kan bruge til f.eks. at producere medicin, bruger man høje temperaturer og højt tryk til mekanisk at bearbejde den komplekse biomasse. I den bearbejdede biomasse er der stadig en stor del af biomassen som er ubrugelig for de fleste celler f.eks. pga. en meget kompleks struktur, men der bliver også frigivet stoffer, der er giftige for cellerne. Et af de største problemer kommer fra giftstoffet furfural, som hæmmer væksten af celler markant, og ved højere koncentrationer faktisk kan dræbe cellerne. Hvis væksten af celler bliver hæmmet – eller hvis cellerne bliver dræbt – giver det sig selv, at cellerne ikke fungerer godt som små (celle)fabrikker. Samtidigt er over halvdelen af den ubrugelige biomasse lignin, som de færreste celler kan nedbryde.
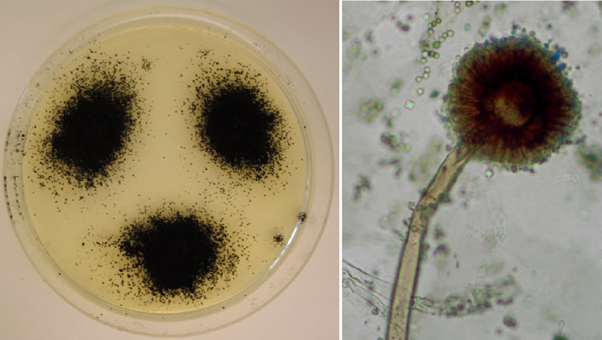
Vi kan dog løse dette ved at bruge svampen Aspergillus niger! Denne filamentøse svamp (også kendt som skimmelsvamp) bliver flittigt brugt som produktionsorganisme i industrien, og kan endda nedbryde lignin. På figur 3 kan du se, hvordan A. niger ser ud.
Lav en Google søgning; Hvad kan du finde ud af om A. niger? Hvor trives den (i naturen og i industrien)? Hvilke produkter kan man lave vha. A. niger?
Kender du andre organismer, der bliver brugt til produktion, f.eks. i den danske industri?
Syntetisk biologi hjælper A. niger
A. niger er følsom overfor furfural, og kan derfor ikke vokse godt på bearbejdede restprodukter fra land- og skovbrug, som jo indeholder store mængder furfural. Det er her syntetisk biologi kommer i spil; ved hjælp af genmodificering kan vi skabe en ny stamme af A. niger, der kan nedbryde furfural (så svampen kan overleve), og samtidigt udnytte biomassen (også lignin!) til produktion af nyttige produkter, såsom medicin, farvestoffer, smagsstoffer og meget mere.
Men hvordan kan man mere præcist få en skimmelsvamp til at være modstandsdygtig overfor giftstoffer, tænker du måske? Det er jo heller ikke smart, hvis skimmelsvampen bruger en masse energi på at bekæmpe furfural, hvis den ikke har brug for det.
Det er nemlig sådan, at mængden af furfural varierer mellem biomassetyper. Derfor ville det være smart hvis generne, der er ansvarlige for at nedbryde furfural, kun aktiveres når furfural rent faktisk er til stede. Men hvordan kan man opnå en sådan regulering af generne? Man kan eksempelvis bruge specialiserede transkriptionsfaktorer!
Transkriptionsfaktorer tænder eller slukker for genekspression
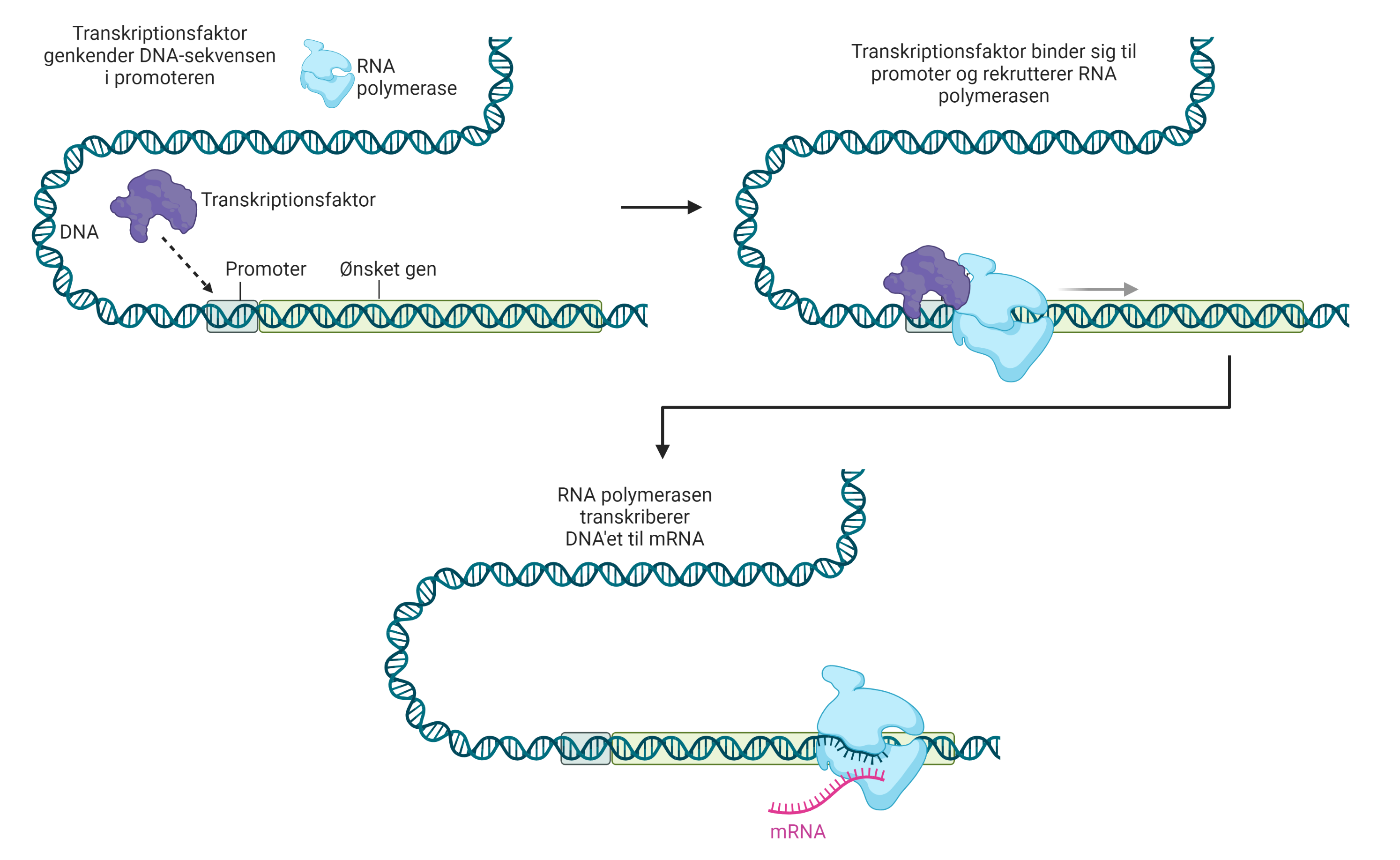
Et gen bliver altid transkriberet fra DNA til mRNA startende fra genets promoter. DNA’et der udgør en promoter, kan tiltrække helt særlige proteiner, der binder til promoteren. Disse proteiner kaldes transkriptionsfaktorer. Transkriptionsfaktorer kan være meget specialiserede til bestemte promoterer, hvor de kan binde til en helt speciel DNA-sekvens. Binding af disse transkriptionsfaktorer til promoteren på DNA’et er med til at guide RNA polymerase til også at binde DNA’et, så det kan begynde at transkribere DNA’et til mRNA. En sådan transkriptionsfaktor kaldes også en aktivator. Der findes også transkriptionsfaktorer, der blokerer for transkriptionen; dem kalder vi for repressorer. På figur 4 kan du se, hvordan transkriptionsfaktorer virker.
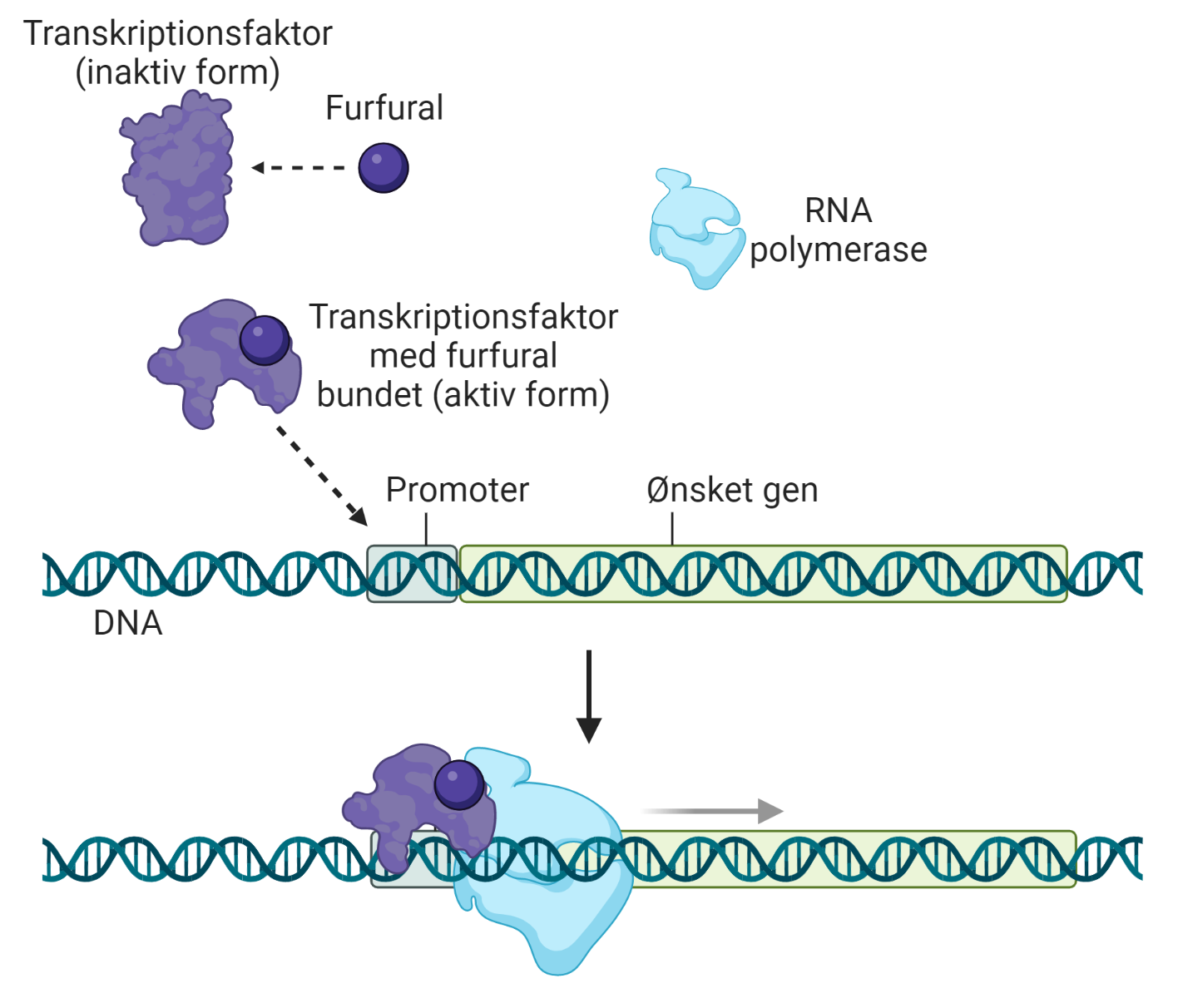
En måde at kontrollere udtrykket af gener, der kan nedbryde furfural, er ved f.eks. at designe en transkriptionsfaktor, der kan genkende og binde furfural, og som skifter form, når furfuralen binder sig. Når transkriptionsfaktoren har skiftet form, kan den binde sig til en specifik DNA-sekvens, som man vha. syntetisk biologi har indsat foran et relevant gen i A. niger.
Dette “relevante gen” kan f.eks. kode for et farvestof. Hvis man kan se farvestoffet ved man altså, at genet er blevet udtrykt, og derfor at der er furfural tilstede.
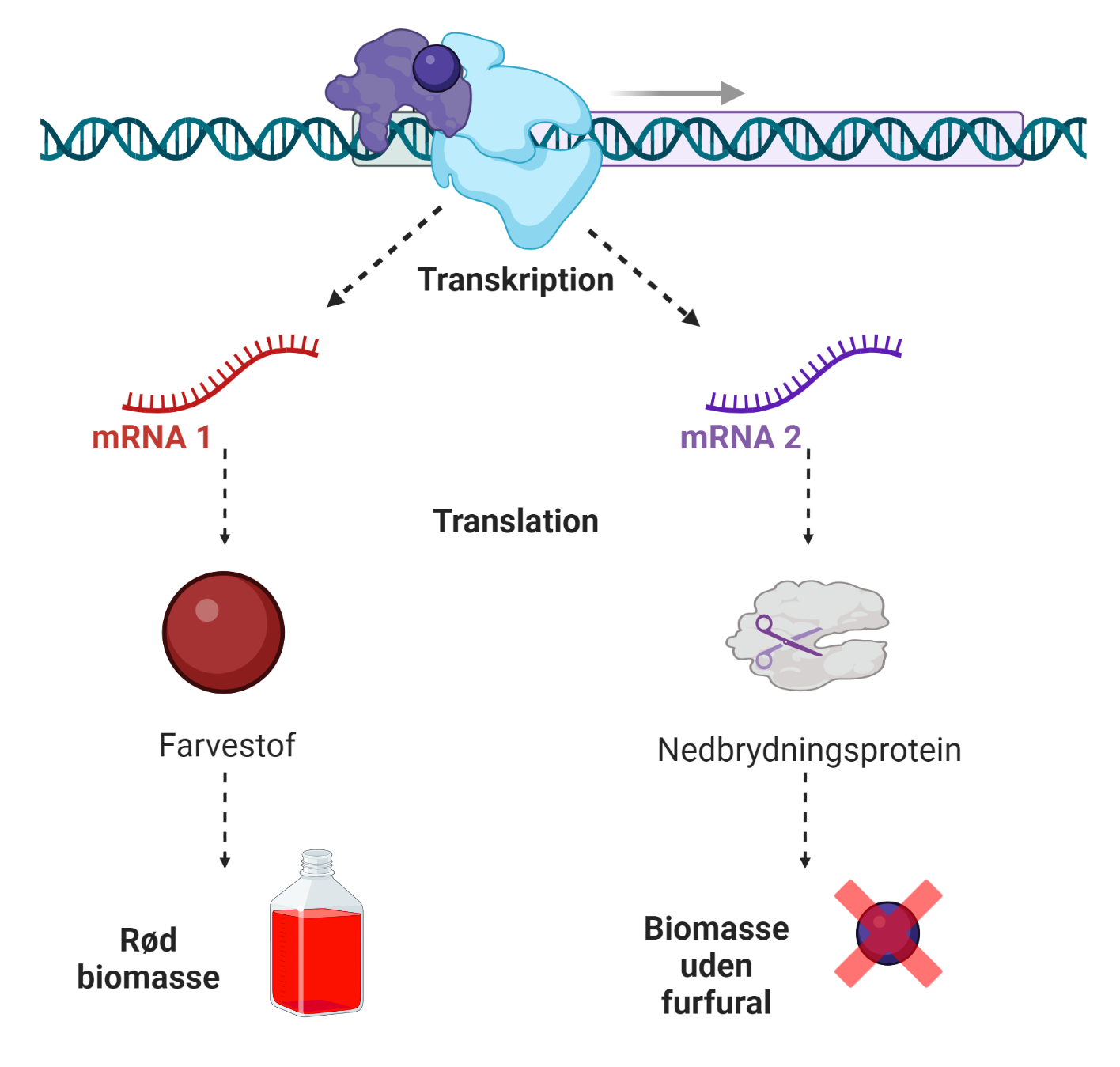
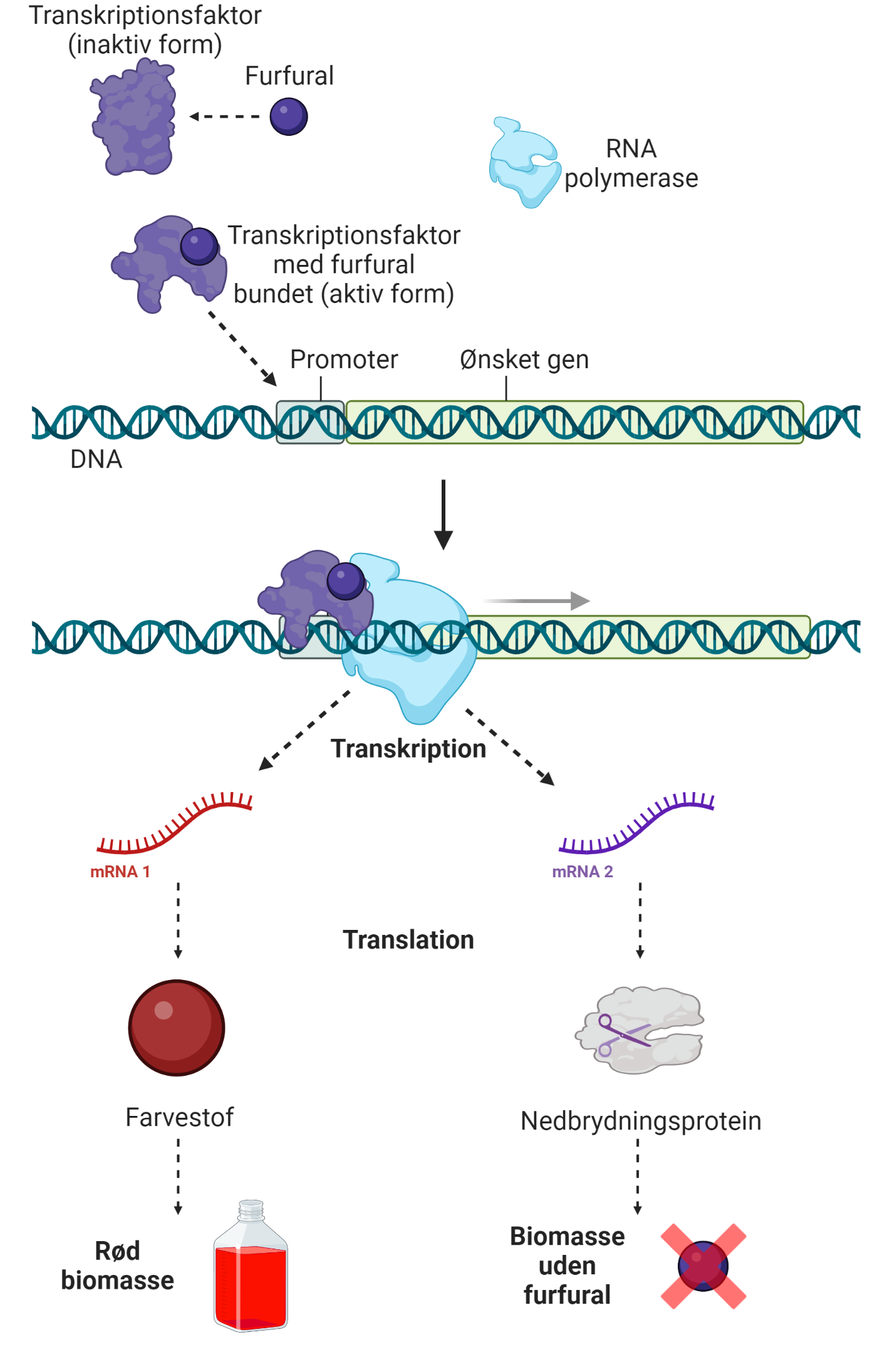
Genet kan også kode for et protein, der kan nedbryde furfural. På den måde kan man styre produktionen af nedbrydningsproteinet, for det bliver kun dannet, når der netop er furfural til stede. Det er ret smart, for så skal cellen ikke bruge unødvendigt meget energi på at producere nedbrydningsproteiner når de ikke skal bruges. På figur 5 kan du se, hvordan en furfural-aktiveret transkriptionsfaktor kan virke.
Man kan altså skabe en celle, der er i stand til visuelt at markere når furfural er tilstede, og som også kan skabe proteiner, der kan nedbryde furfural, når netop furfural er tilstede. Man kalder et system, der kan opfange/detektere stoffer og derefter give et signal (f.eks. produktion af et farvestof eller nedbrydningsprotein) for en biosensor – fordi det er et biologisk system, der “sanser” noget.
Hvis cellen er i stand til at nedbryde furfural, og samtidigt bruge biomassen til at lave medicin, kan vi altså indføre restprodukter fra skov- og landbrug helt i toppen af den bioøkonomiske værdipyramide fra figur 1. Efterfølgende kan restprodukter fra medicinproduktionen bruges til at skabe produkter af lavere værdi, og helt til sidst kan restprodukterne bruges til at skabe varme og energi.
På denne måde kan vi altså få en meget mere effektiv brug af vores ressourcer, og passe bedre på vores allesammens Jord.
Hvilke problemer kan du se, ved at genmodificere A. niger til at omdanne furfural? Hvilke muligheder giver det, at genmodificere A. niger til at omdanne furfural?
Kan du komme på andre stoffer, som det kunne være smart at nedbryde?