Gelelektroforese
Gelelektroforese: Adskillelse af DNA eller protein
Gelelektroforese er en adskillelsesteknik, der kan bruges til at separere forskelligt DNA eller protein i en gel. Det gør det bl.a. muligt forholdsvis præcist at måle enten antallet af basepar i en DNA-prøve eller længden af forskellige proteiner.
Adskillelse af forskellig DNA og proteiner er også nyttigt til oprensning fra en prøve. Fx kan man mindske risikoen for at bruge fejldannet DNA ved gensplejsning med DNA, man selv har fremstillet, hvor der samtidig er blevet dannet andre længder DNA end det korrekte; man adskiller simpelthen de forskellige længder og skærer den rigtige længde ud af gelen. Gelelektroforese bruges derfor ofte på flere forskellige stadier i udviklingen af en ny genmodificeret organisme.
Adskillelse af DNA
I gelelektroforese af DNA udnyttes den negative ladning, som DNA har, til at adskille DNA af forskellig længde i en prøve. Den negative ladning stammer fra phosphatgrupperne i hvert nukleotid af DNA’et. De geler, der bruges, er faste og gennemsigtige. De støbes ud fra en opløsning af nogle særlige molekyler fx agarose.
DNA-prøven tilsættes i en brønd (fordybning) for enden af en gel, og der tilsluttes derefter elektrisk spændingsforskel. Herved skabes en frastødende negativ pol ved DNA-prøven og en tiltrækkende, positiv pol i den anden side af gelen (figur 29). DNA’et vil altså nu trække gennem gelen mod den positive side. De mikroskopiske huller i gelen gør bevægelsen sværere for DNA’et, jo længere det er. Derfor løber de korte DNA-molekyler hurtigere igennem end de længere.
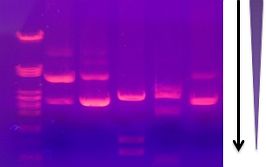
Efter en gelelektroforese vil DNA’et derfor ligge sorteret i forskellige bånd efter antal basepar (alle, der er 600 basepar, ligger fx lige oven i hinanden).
Flere forskellige stoffer kan gøre DNA’et synligt for fotografering. Ofte brugt er ethidiumbromid, som binder sig til DNA’et, der herved bliver synligt i ultraviolet lys, som bruges ved fotograferingen af den færdige gel. Man kan køre flere prøver ved siden af hinanden i en gelelektroforese, hvor den yderste typisk vil være en markør, der indeholder nogle allerede kendte længder, så man kan sammenligne med prøverne.

Figur 29. Princippet i DNA gelelektroforese, hvor de forskellige størrelser DNA adskilles i en gel. Gelen ligger i et kar med en buffer-væske.
Adskillelse af protein: SDS-PAGE og pI
Gelelektroforese af protein bruges til at adskille forskelligt protein, fx efter proteinernes længde.
Modsat DNA har proteiner ofte meget indviklede tredimensionelle strukturer, der derfor vil være afgørende for, hvor hurtigt de forskellige proteiner bevæger sig igennem gelens mikroskopiske huller. For at kunne bestemme længden, skal det imidlertid kun være proteinernes længde, der afgør hastigheden, og man foretager derfor en denaturering af proteinet med SDS (natriumdodecylsulfat). I denaturingen udfolder SDS-molekylerne proteinet og binder sig jævnt langs det. Da SDS er et negativt ladet molekyle, får hver proteinkæde en negativ ladning svarende til dens længde. Den nye, negative ladning overdøver i styrke klart en evt. positiv ladning, som proteinet havde inden. Dermed resulterer SDS-behandlingen i et udfoldet protein, hvis længde kan måles.
Man bruger en polyakrylamid-gel (PAGE) til gelelektroforese af protein, men princippet er det samme som ved DNA-gelelektroforese: En negativ og positiv elektrisk pol driver proteinprøven gennem gelen, og hastigheden gennem de mikroskopiske huller afhænger af proteinets længde. Derfor opnår man en længdeafhængig adskillelse, som giver sig til syne, når proteinerne til slut farves. Størrelsen af proteiner opgøres gerne i kDa (kilodalton), som svarer til massen i kilogram af et mol af proteinet.
Adskillelse ved isoelektrisk punkt pI
Proteiner har andre forskellige egenskaber, som kan bruges til at sortere og adskille dem i en gelelektroforese. Én er deres isoelektriske punkt (pI), som er den pH-værdi, hvor proteinets aminosyrer samlet set vil være neutrale i ladning. Hvis pH i opløsningen kommer under dette punkt, bliver der flere positive ladninger end negative på proteinet, og proteinet vil fremstå positivt. Modsat bliver proteinet samlet set negativt, hvis opløsningens pH kommer over pI.
Man kan adskille forskellige proteiner efter deres pI-værdi i en gel, hvor pH-værdien på langs gradvist stiger fra lav til høj. I den lave pH-ende sætter man en positiv elektrisk pol, og i den høje pH-ende en negativ pol. For når et protein befinder sig ved pH-værdier over dets pI, er det som nævnt negativt i samlet ladning, og det vil derfor automatisk drive mod dets pI-værdi (der jo er i retning mod den positive pol og lavere pH-værdier). Denne drivning vil fortsætte, lige indtil proteinet når den pH, der er lig dets pI-værdi. Ved denne pH er dets samlede ladning nul, og proteinet ligger derfor stille, upåvirket af elektrisk tiltrækning! Dermed vil proteinerne altså langsomt placere sig på den position i gelen, hvor pH er lig dets pI.

Figur 30. Princippet i en 2D gelektroforese af protein, hvor proteinerne først adskilles i 1. dimension efter deres isolelektriske punkt og dernæst i 2. dimension efter deres størrelse med SDS.
I en 2D gelelektroforese kan man adskille en proteinprøve efter både pI og længde. På den ene led af gelen adskiller man først efter pI-værdi, og når proteinerne er sorteret efter det, vender man gelen og tilsætter SDS, så de nu på den anden led kan blive adskilt efter længde (figur 30 og 31).
Resultatet er således en gel med prøvens forskellige proteiner principielt spredt ud over hele gelen. Hvis to forskellige proteiner i prøven fx havde samme pI-værdi og derfor ikke blev adskilt efter denne egenskab, er det sandsynligt, at de har forskellig længde og derfor vil blive adskilt på den anden led.
Eksempler på brug af gelelektroforese:
Gelelektroforese er meget ofte brugt i arbejde, hvor DNA eller protein håndteres eller synliggøres. Den anvendes fx ved:
- Southern blotting (DNA)
- Western blotting (Protein)
- Restriktionsskæring
- PCR

Figur 31. 2D gelelektroforese af proteiner fra humant blodplasma. Proteinerne er på horisontalt led adskilt efter isoelektrisk punkt (pH) og på vertikalt led adskilt efter størrelse (kDa). Gel fra Institut for Systembiologi, DTU.