Enzymer – naturens værktøj
Dette afsnit er det fjerde i Biotech Academys serie om enzymer til folkeskolen.
Funktion og egenskaber
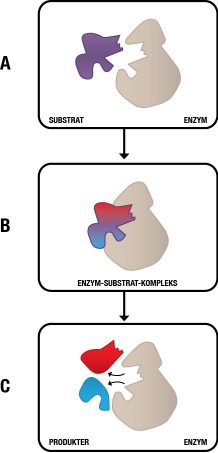
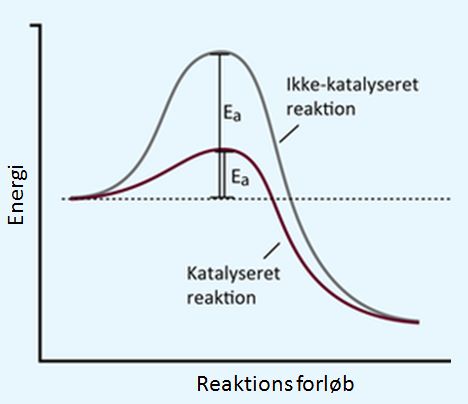
Enzymer findes i alle organismer, lige fra encellede bakterier til flercellede planter og dyr. Enzymer er nogle af livets vigtigste dele og uden enzymer ville liv, som vi kender det, ikke kunne eksistere. Enzymer er en del af stort set alle processer i cellen. I mennesket bliver enzymer bl.a. brugt, når maden skal fordøjes, eller når en muskel skal bevæge sig. Enzymer er naturens katalysatorer. En katalysator er et molekyle, der kan forøge hastigheden af kemiske reaktioner, uden at katalysatoren selv bliver ændret. Dette betyder, at enzymer kan hjælpe reaktioner på vej, uden at de selv bliver ødelagt eller forsvinder.
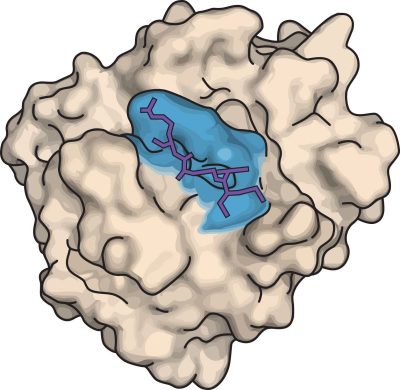
Fordi et enzym er et protein, folder det på en bestemt måde, så det får en helt særlig tredimensionel form, der har stor betydning for dets funktion. Når enzymet er foldet, har det et såkaldt aktivt sæde. Det aktive sæde er som regel formet som en kløft eller et hul på overfladen af enzymet. Det er her katalysen foregår. Det er kun nogle bestemte molekyler, der passer til et enzyms aktive sæde. Disse molekyler kaldes for enzymets substrater (se figur 6).