Kræftstamceller
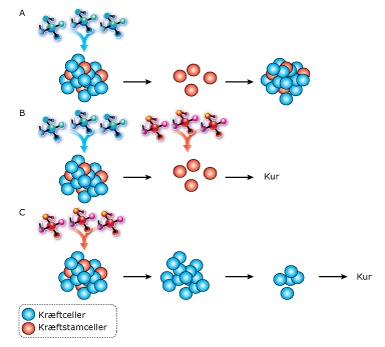
I starten af det 20. århundrede var infektionssygdomme (sygdomme hvor bakterie-infektion er årsagen til sygdommen) ofte dødelige. Nu om dage er disse og en lang række andre sygdomme ofte relativt nemme at behandle, hvilket har medført en enorm forøgelse af den gennemsnitlige levealder i den vestlige verden. Denne forøgelse i levealder har gjort, at hjerte-/karsygdomme og kræft nu om dage er de sygdomme, som hvert år koster flest menneskeliv, idet disse sygdomme oftere opstår hos ældre personer. Mens der siden 1960’erne er sket store fremskridt i behandlingen af hjerte-/karsygdomme (ift. at den forventede levealder for en patient er steget med adskillige år), har den medicinske kræftbehandling haltet bagefter. Hver gang aviserne skriver, at der er sket et enormt fremskridt i behandlingen af en bestemt kræfttype, er dette fremskridt sjældent større, end at den gennemsnitlige levealder for denne type kræftpatienter er øget med et halvt år. Ydermere oplever mange kræftpatienter tilbagefald, efter de egentligt er erklæret “raske”. F.eks. er der for danske patienter med tyktarmskræft, hvor denne kræft har spredt sig til lymfeknuderne, kun 47 % i live fem år efter endt succesfuld behandling (hvor patienten blev “kureret”). Selvom den traditionelle kræftmodel, som er beskrevet i de første artikler i Mennesket på en DNA-mikrochip, forsøger at forklare dette fænomen, er det sandsynligt, at modellen ikke til fulde kan forklare den store kompleksitet af kræft. En ny teori, som forsøger at forklare årsagen til patient tilbagefald samt flere af kræftens karakteristika er Kræftstamcelleteorien, som vil blive introduceret i denne artikel.
Stamceller
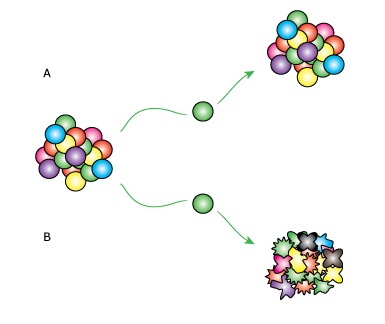
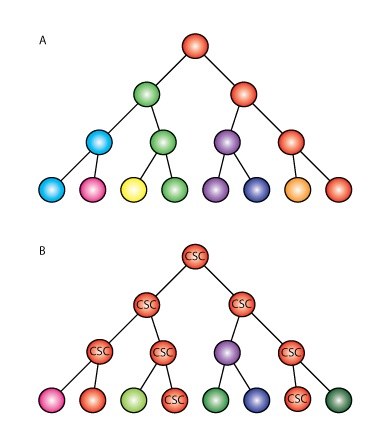
Inden beskrivelsen af selve kræftstamcelleteorien er det relevant kort at forklare, hvad en stamcelle er. En stamcelle er en type celle, som besidder den egenskab, at den kan dele sig asymmetrisk. Dette vil sige, at den kan dele sig til nye stamceller, men også til andet mere differentieret celleafkom. Kroppens stamceller virker derfor som et lager af ”moderceller”, som kan opretholde kroppens cellepopulation (der dør hele tiden celler i vores krop af forskellige årsager, og det er derfor nødvendigt med tilførsel af nye, friske celler). I modsætning til alle kroppens andre celler er stamceller desuden i stand til at forlænge deres telomerer i enden af deres kromosomer vha. enzymet human telomerase revers transkriptase (hTERT). Telomererne er ikke-kodende DNA, som sidder i enden af hvert kromosom for at beskytte de rigtige gener. Ved alle celledelinger mister hvert kromosom nemlig et stykke af DNA’et, og uden telomererne ville dette stykke blive taget fra generne. Det vil efter et antal celledelinger medføre, at cellen ikke længere kan fungere. Cellen vil derpå undergå apoptose (programmeret celledød). Telomererne virker derfor som en slags ”bufferzone”, der bevirker, at en celle kan dele sig mange gange uden at påvirke generne. Vha. enzymet hTERT kan stamcellerne efter hver celledeling forlænge deres telomerer, således at deres gener er beskyttede. Stamcellen kan derfor i princippet leve uendeligt. Ydermere bør det nævnes, at stamceller er langsomt delende celler, og at de pga. deres hTERT-enzym ofte lever i mange år.
Det interessante ved kræftceller er, at de på nogle områder minder om stamceller. Bl.a. er det i mange typer kræft blevet påvist, at en subpopulation af kræftcellerne også er i stand til at producere hTERT, hvilket giver dem den egenskab, at de også kan leve uendeligt.