Stamcelleterapi og udviklingsbiologi


I denne artikel forklares, hvad en stamcelle er, og hvordan man håber, at stamcelleforskningen vil give resultater, der kan bruges til at helbrede en lang række sygdomme i fremtiden. Herefter gennemgås de grundlæggende teorier inden for udviklingsbiologien, der beskriver, hvordan et foster udvikles på molekylært niveau. Det beskrives til sidst, hvordan forskning i udviklingsbiologi er nødvendig for at kunne lave effektive behandlinger af sygdomme med stamceller.
En stamcelle er en celle, der kan differentiere sig (dele sig og udvikle sig) til mange forskellige celletyper i kroppen – man kan sige, at den er stamfader til kroppens celler. Både det befrugtede æg og de første celler, der dannes, når ægget deler sig, er stamceller, da de kan differentiere sig til alle kroppens celler.
Det befrugtede æg deler sig flere gange og kaldes en blastocyst, når det består af ca. 100 celler. Blastocysten består af to forskellige celletyper, så der er allerede her sket en differentiering. Den indre cellemasse i blastocysten består af stamceller, som udvikler sig til det egentlige foster. Man kan få den indre cellemasse til at vokse i en petriskål i laboratoriet, og det er på den måde, at en kultur af embryonale stamceller kan etableres. Det er disse celler, der normalt benyttes, når der tales om ”forsøg med stamceller” eller ”ES-celler”. De embryonale stamceller bevarer deres funktion, når de dyrkes i laboratoriet. De rummer således muligheden for at kunne differentiere sig til alle kroppens mere end 200 kendte celletyper. Det er dog vigtigt at understrege, at de alene ikke kan danne et nyt menneske, da de ikke kan differentiere sig til cellerne i navlestrengen og moderkagen.
Rigtig mange af de alvorligste sygdomme skyldes, at bestemte celler i kroppen dør eller ikke fungerer normalt. Således er betaceller døde i en diabetespatient, mens bestemte nerveceller er syge eller døde ved Parkinsons sygdom. Hvis disse celler erstattes med nye raske celler, vil patienten blive helbredt. Denne metode, hvor syge celler erstattes med raske, kaldes celleterapi, og det er bevist, at den virker i en lang række tilfælde.
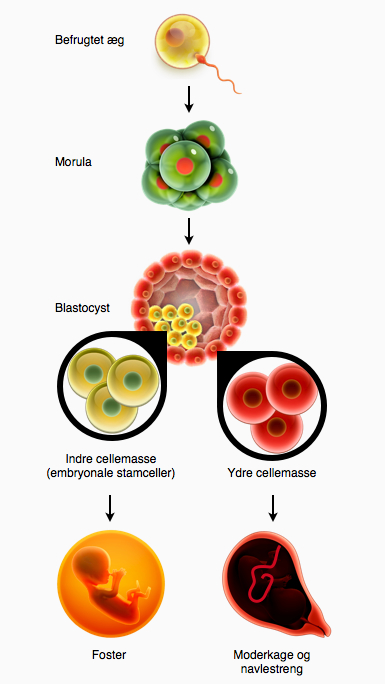
Figur 11. Udvikling fra befrugtet æg til foster. Et befrugtet æg deler sig og udvikler sig til en blastocyst, hvor cellerne er differentieret til to forskellige typer. Den indre cellemasse i blastocysten, udvikler sig til alle celler i kroppen, bl.a. hjertet, nervesystemet og immunsystemet. De ydre celler udvikler sig til moderkage og navlestreng, der supplerer det udviklende foster med næring og ilt.
Ligesom med organtransplantationer kan raske celler overføres fra et menneske til et andet. Men der er desværre kun nok donorer til at behandle en brøkdel af dem, som kunne have glæde af det. Forskere forsøger derfor at finde en metode til at lave store mængder raske celler, der kan erstatte de syge i patienterne. Da embryonale stamceller har muligheden for at blive til alle celler i kroppen, er det oplagt at forsøge at lave dem om til en bestemt celletype (terapeutiske celler) og derefter erstatte de syge celler i en patient. Denne fremgangsmåde kaldes celleterapi med embryonale stamceller eller blot stamcelleterapi.
Det store problem er, at det er meget kompliceret at lave stamceller om til diverse terapeutiske celler uden for kroppen. Når fosteret udvikler sig, er der et komplekst samspil mellem fosterets og moderens celler, og forskellige signalproteiner får cellerne til at udvikle sig i forskellige retninger. Som beskrevet er det målet at kunne lave stamceller om til bestemte terapeutiske celler uden for kroppen. For at det skal lykkes er det nødvendigt at finde ud af præcis, hvad der sker i kroppen, når bestemte celler dannes i et udviklende foster. Forskningen i udviklingsbiologi, er derfor utrolig vigtig for at kunne lave stamceller om til forskellige terapeutiske celler og, på længere sigt, helbrede mange millioner mennesker for nogle af de alvorligste sygdomme, vi kender.
Det er utroligt at forestille sig, at en enkelt celle – det befrugtede æg – kan udvikle sig til et helt nyt menneske. Formålet med udviklingsbiologien er netop at finde ud af, hvordan det befrugtede æg bliver til alle de forskellige specialiserede celler i vores krop, og hvordan cellerne organiseres, så de ligger de rigtige steder.
Det hele starter med at et æg befrugtes med en sædcelle. Det befrugtede æg deler sig og udvikler sig til en blastocyst, hvor cellerne er differentieret til to forskellige typer, den indre og ydre cellemasse. Den videre differentiering af den indre cellemasse kaldes gastruleringsprocessen, hvor disse celler organiseres i et indre, mellem og ydre lag. Det er allerede på dette stadie forudbestemt, hvilke celler de forskellige lag kan blive til. Det indre lag, endoderm, kan blive til blandt andet lunge-, tarm-, lever- og bugspytskirtelceller (herunder betaceller). Det mellemste lag mesoderm, udvikler sig til blodceller, knogleceller, muskelceller m.fl. Det ydre lag, ectoderm bliver blandt andet til nerve- og hudceller.
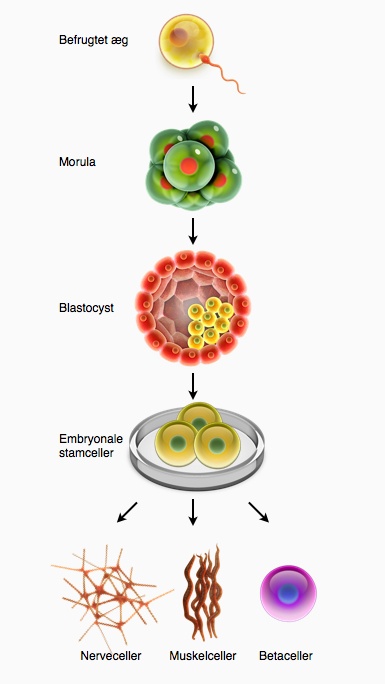
Figur 12. Fremskaffelse af embryonale stamceller. Den indre cellemasse fra en blastocyst kan dyrkes i laboratoriet. Den kaldes så en kultur af embryonale stamceller. Embryonale stamceller kan blive til alle de celletyper, der findes i kroppen, hvis der vel at mærke tilsættes de rigtige stoffer til cellerne. Hvis de dannede celler kan bruges til at behandle en sygdom, kaldes de terapeutiske celler. Eksempler på tre celletyper der kan dannes fra embryonale stamceller er vist.
Ud fra denne viden som udviklingsbiologerne har fundet frem til, kan det konkluderes, at det første skridt på vejen til dannelsen af f.eks. betaceller fra stamceller, er at lave endodermale celler. Det er derfor nødvendigt at se på hvilke signalproteiner, der påvirker netop dannelsen af det indre lag, endodermen. I den sammenhæng er det vigtigt at vide, hvilken rolle signalproteiner spiller for hele fosterudviklingen.
Allerede tidligt i udviklingen begynder cellerne at danne signalproteiner. Det befrugtede æg og de første mange celler, der dannes fra det, bliver meget påvirket af hvilke signaler, der er til stede omkring dem. Disse signaler er afgørende for, hvordan en celle udvikler sig. Således kan bindingen af bestemte signalproteiner til receptorer på en celles overflade, få cellen til at begå kontrolleret selvmord, dele sig, bevæge sig, eller differentiere sig til en ny celletype. En receptor kan beskrives som et nøglehul, mens signalproteinet er en nøgle: Kun hvis den rigtige nøgle sættes i låsen, fås en reaktion.
Flere af disse signalproteiner informerer cellerne om, hvor de befinder sig: foran, bagved, til højre eller til venstre i hvad der senere bliver til fosteret. Dette foregår ved, at der i forenden af celleklumpen (f.eks. den ende der holder celleklumpen fast til livmoderen), dannes et bestemt signal. Dette signal fortæller cellerne, hvor tæt de befinder sig på forenden af celleklumpen: Hvis de er tæt på, er signalet stærkt, hvis de er langt væk, er det svagt. På samme måde udskiller cellerne i venstre side af celleklumpen et bestemt signalprotein.
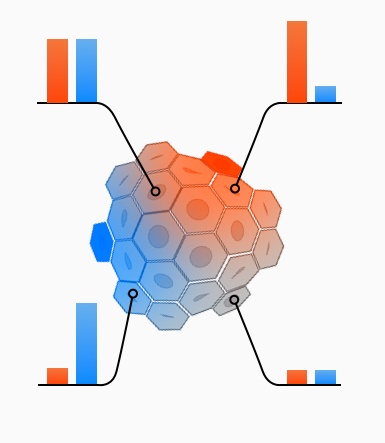
Figur 13. Koncentrationen af signalproteiner varierer i blastocysten. Figuren illustrerer, hvordan forskellige celler i blastocysten udsender bestemte signalproteiner (her vist med rød og blå farve). Koncentrationen af de to signalproteiner varierer meget i de forskellige dele af blastocysten, hvilket også kan ses af de fire grafer. signalproteinerne påvirker cellerne til at differentiere sig i forskellige retninger.
Når disse signaler opfanges af cellerne, reagerer de på bestemte måder. Hvis en celle f.eks. ligger foran til højre i celleklumpen på figuren, vil den modtage kraftige signaler fra cellerne foran, men kun svage signaler fra cellerne til venstre. I cellernes arvemasse er indkodet, præcis hvordan de skal udvikle sig ved modtagelsen af bestemte signaler, og cellerne i et bestemt område udvikler sig derfor ens. Celler, der kun modtager det blå signal, vil altså udvikle sig anderledes end celler, der modtager både det røde og det blå signal. Det skal understreges, at der i et udviklende foster er mange flere signalproteiner end de her angivne, og at farverne blot er for illustrationens skyld.
Det kan også være altafgørende, hvor kraftigt signalet er. F.eks. kan en meget høj koncentration af et signalprotein føre til én reaktion, mens en mindre kraftig koncentration, kan føre til en anden. I et bestemt område af det udviklende foster, begynder der f.eks. at dannes et signalprotein, der er vigtigt for dannelsen af bugspytkirtlen.
Hvis dette signalprotein modtages kraftigt (af celler der er tæt på), begynder cellerne at udvikle sig til et forstadium af bugspytkirtlen.
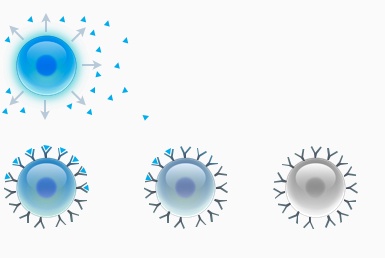
Figur 14. Cellesignalering bestemmer cellernes udvikling. En celle udsender et signal (små trekanter). Dette signal opfanges af andre celler, men jo længere væk de er, jo mindre signalprotein modtager de. Det er helt afgørende for cellernes udvikling, hvor kraftigt de modtager et bestemt signal. De tre nederste celler udvikler sig derfor helt forskelligt pga. den forskellige koncentration af signalprotein, der binder sig til dem.
Hvis signalproteinet modtages svagt, signalerer det til gengæld det modsatte: ”du skal ikke blive til en bugspytkirtelcelle, da andre celler allerede er i gang med dette”. Det kan føre til, at de celler der modtager det svage signal, udvikler sig i en anden retning eller begår kontrolleret celleselvmord.
Modtagelsen af bestemte signaler kan også føre til, at cellen selv begynder at udsende signaler. På den måde opstår der et komplekst signalnetværk, hvor celler signalerer til hinanden og udvikler sig efter hvilke signaler, de modtager. Det er dette utrolig komplekse netværk af signaler, der sørger for, at alt i det nye menneske dannes de rigtige steder og med de rigtige størrelser.
Alle celler i kroppen indeholder præcis de samme gener i deres DNA, så hvordan kan de udvikle sig forskelligt? Det skyldes, at det i cellerne er meget forskelligt, hvilke gener der er aktiveret. F.eks. har alle celler i kroppen genet for insulin, men kun i betacellerne er det aktivt. Om et gen er aktivt, kan reguleres af såkaldte transkriptionsfaktorer. En transkriptionsfaktor er et protein, der kan binde til et gen og derved bestemme, om genet bliver udtrykt. Det ses ofte, at et signalprotein binder til en receptor på en celle, hvorefter en bestemt transkriptionsfaktor aktiveres. Transkriptionsfaktoren bestemmer herefter, om et bestemt gen aktiveres eller ej. Der er to forskellige former for transkriptionsfaktorer, hvoraf den mest almindelige kaldes en aktivator.
En aktivator binder til bestemte gener og sørger for at de bliver udtrykt, således at genet kun udtrykkes, når aktivatoren er til stede. En repressor, vil derimod forhindre, at et bestemt gen bliver udtrykt. Genet vil kun blive udtrykt, hvis repressoren ikke er til stede. Transkriptionsfaktorer kan altså meget præcist kontrollere, hvilke gener der er aktive i en celle.
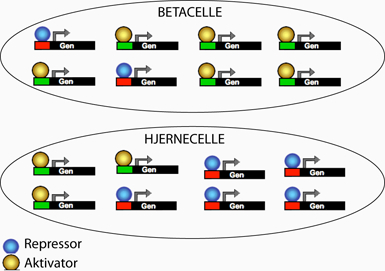
Figur 15. Cellerne fra et menneske indeholder samme arvemasse og adskiller sig fra hinanden fordi der er forskel på hvilke af cellernes gener, der er aktiveret. Alle celler i kroppen har det samme DNA. Det der gør dem forskellige, er hvilke gener, der er aktive i cellerne. Det er transkriptionsfaktorer (aktivatorer og repressorer) der direkte styrer, hvilke gener der bliver udtrykt ved at binde sig til DNA’et. Som eksempel er her vist, hvordan en hudcelle og en betacelle har de samme gener, men udtrykker forskellige af dem.
Der er f.eks. et bestemt signalprotein, som aktiverer en transkriptionsfaktor, der binder sig både til insulin-genet og til genet for et glukosetransportprotein. Denne transkriptionsfaktor sørger for at de to gener bliver udtrykt, og fungerer som en aktivator. Det er lige præcis dette bestemte signalprotein, som forskerne prøver at finde. Dog er det mere kompliceret end som så. signalproteinet virker nemlig kun på helt bestemte celler, der har modtaget den helt rigtige rækkefølge af signalproteiner, siden cellerne var et befrugtet æg. Forskerne er altså nødt til at finde hele den række af signalproteiner, der kan omdanne en stamcelle til en bestemt terapeutisk celle.
Vejen fra en stamcelle til en betacelle beskrives vha. følgende: Først skal der dannes en endodermal celle vha. bestemte signalfaktorer. Den endodermale celle påvirkes herefter til at blive til en umoden celle, der udtrykker transkriptionsfaktoren Pdx1. Et bestemt signalprotein laver den endodermale celle til en pdx1-positiv umoden celle, mens et andet signalprotein, laver den til en levercelle.
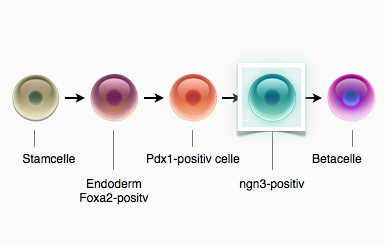
Figur 16. Udvikling fra en stamcelle til en betacelle. Det bliver din opgave at finde de signalproteiner, der kan påvirke en stamcelle til at følge denne udvikling. Derpå skal du afprøve dem i det virtuelle laboratorium.
Den Pdx1-positive celle har muligheden for at blive til alle cellerne i bugspytkirtlen bl.a. en neurogenin3-positiv celle (ngn3), der igen har muligheden for at blive til alle hormonproducerende celler i bugspytkirtlen, men ikke til andre. Det er lykkedes forskere at få dannet en ngn3-positiv celle, men ikke at videredifferentiere den til en funktionel betacelle.
Man kan undre sig over, hvorfor der overhovedet eksisterer stamceller, Det ville da være meget nemmere hvis alle celler i kroppen bare kunne dele sig. Et stort problem er, at jo mindre differentieret en celle er, jo større er sandsynligheden for, at den kan forårsage kræft.
Kræft opstår, når kroppens egne celler ikke længere kan kontrolleres. De begynder at vokse uhæmmet, og beskadiger derved de raske celler i kroppen. For at forhindre kræft, er der en række kontrolmekanismer, som sørger for, at kroppens celler ikke deler sig uhæmmet. En af disse kontrolmekanismer er, at kun stamceller har muligheden for at dele sig uendeligt. Alle andre celler i kroppen kan enten slet ikke dele sig eller kun dele sig et begrænset antal gange. Stamceller kan danne teratomer – en speciel kræftsvulst, som indeholder mange forskellige typer væv. Det er faktisk ”kvalitetsstemplet” på en embryonal stamcellekultur, at den kan danne forskellige væv fra alle tre kimlag (endo- meso- og ectoderm) i teratomaer, når den indsprøjtes i såkaldt ”nøgne mus”. Det er mus, der har fået fjernet deres immunforsvar, så de ikke afstøder fremmede celletyper, og dermed kan bruges til forsøg som dette. Det er af samme grund utrolig vigtigt, at være sikker på, at der ikke er nogen udifferentierede stamceller tilbage, når der laves terapeutiske celler fra stamceller. De tilbageværende stamceller vil medføre en stor risiko for kræft. Det er nødvendigt med omfattende kontrolmekanismer, som sikrer dette, så behandlinger, der er lavet til at helbrede én sygdom, ikke giver en meget seriøs bivirkning, nemlig at patienterne får kræft.