Antistoffer som lægemidler
Denne underside udgør femte del af teorien for Biotech Academys materiale om Immunforsvaret.


Denne underside udgør femte del af teorien for Biotech Academys materiale om Immunforsvaret.
Vaccinationer er én anvendelse af immunologien til sygdomsbekæmpelse. Men immunologiens andre facetter bliver i stigende grad også anvendt. Det drejer sig især om antistoffer, der både kan bruges i laboratoriearbejdet eller direkte som lægemidler uden om immunforsvaret. I det følgende afsnit vil nogle antistoffer, der bliver brugt som medicin i behandlingen af mennesker, blive beskrevet.
Antistoffer er den dyreste medicingruppe, der bliver brugt i dag. Den høje pris for de antistoffer, skyldes bl.a. at en stor del af antistoffer stammer fra oprenset blod fra immune personer. Det kan være personer, der enten har overlevet en infektion, eller som er blevet vaccineret mod et bestemt antigen. Antallet af disse personer, der samtidig er villige til at donere blod, er begrænset, og prisen er derfor høj. Syntetisk udvikling af antistoffer er derfor et vigtigt fremskridt for videnskaben, og forhåbentlig kan man herigennem sikre en billigere forsyning af antistoffer i fremtiden.
Rhesus-antigener er en samlet betegnelse for omkring 50 forskellige antigener, som findes på de røde blodlegemer hos de fleste. De røde blodlegemer transporterer oxygen rundt i kroppen til alle vores celler. Rhesus-egenskaben blev opdaget i rhesusaber før 2. verdenskrig, og antigenerne har fået deres navn herfra. Rhesus-antigenerne er meget ”immunogene”, hvilket vil sige, at de har en stor evne til at aktivere immunforsvaret og stimulere dannelsen af anti-Rhesus-antistoffer.
Den farligste type er Rhesus D, eller RhD-antigenet. Det skønnes, at ca. 85 % af den danske befolkning er RhD-positive. Det vil sige, at de alle bærer rundt på RhD-antigener på deres egne celler og vil derfor ikke producere antistoffer mod Rhesus D – de er tolerante over for RhD-antigenet.
På grund af den kraftige immunogenicitet kan der opstå alvorlige komplikationer under blodtransfusion, såfremt der anvendes blod med de modsatte rhesus-egenskaber. En RhD-negativ person vil udvikle antistoffer mod RhD-antigener første gang, denne person modtager RhD-positivt blod ved eksempelvis blodtransfusion – et primært respons finder sted.
Ved en yderligere blodtransfusion med RhD-positivt blod vil de allerede dannede antistoffer, samt hukommelses-B-celler, hurtigt reagere imod de fremmede røde blodlegemer – et sekundært respons. Dette medfører såkaldt ”hæmolyse”, hvor de røde blodlegemer ødelægges og frigør stoffer, som får blodtrykket til at falde. Den RhD-negative patient vil altså både ødelægge de transfunderede blodceller og yderligere påvirke sit blodkredsløb i negativ retning. Det vil i mange tilfælde medføre døden, når der bliver givet forkert blod til en patient.
Der udvises stor påpasselighed ved blodtransfusioner for at undgå rhesus-komplikationer, men også under en graviditet kan der opstå komplikationer. Det sker, når en RhD-negativ moder bærer et RhD-positivt barn (det er muligt, når faderen er RhD-positiv).
Der kan nemlig ske blødning mellem moder og barn under fødslen, og herved blandes små mængder af deres blod. Ved den første graviditet sker der som regel kun det, at moderen får aktiveret sine B-lymfocytter til at danne antistoffer mod RhD. Dette skyldes hovedsageligt, at kontakten med de fremmede antigener oftest først finder sted ved fødslen, kombineret med at det tager uger før kroppen har udviklet immunforsvaret nok til at danne rigeligt med antistoffer.
Komplikationerne opstår ved en efterfølgende graviditet med et RhD-positivt barn, hvor moderens RhD-antistoffer krydser moderkagen og angriber fosterets røde blodlegemer. Cellerne ødelægges, og i yderste konsekvens forårsager det fosterets død. For at forebygge dette giver man så vidt muligt altid RhD-negative mødre, der bærer RhD-positivt foster, små mængder af anti-RhD antistof. De små mængder antistof binder sig til fosterets RhD-antigener, og forhindrer derved, at moderens eget immunforsvar har mulighed for at genkende antigenerne. Dette bevirker, at moderens immunforsvar ikke aktiveres, og hendes B-lymfocytter derfor ikke differentierer til antistofproducerende plasmaceller.
Det skønnes, at der i USA og i Europa i alt finder omkring en million graviditeter sted hvert år, hvor det er nødvendigt at tilføre anti-RhD antistoffer. Dette har store økonomiske konsekvenser.
Respiratorisk Syncytial virus er en virusinfektion, som hvert år gør mange spædbørn syge, og som kræver indlæggelse på hospitalet og behandling. RSV inficerer lungerne og luftvejene. Den smitter meget nemt gennem dråber fra en smittet person opstået ved hoste eller tale. Den kan endda overleve længe på eksempelvis dørhåndtag eller legetøj, hvorved man selv kan blive smittet. Det skønnes, at stort set alle børn tilegner sig sygdommen mindst en gang, før de fylder to år. Ny forskning inden for denne virusinfektion tyder på, at børn, der er særligt hårdt angrebet af virussen, risikerer at udvikle langvarige respiratoriske komplikationer i lungerne, fx astma.
Til for tidligt fødte børn, som er særligt udsatte for at tilegne sig sygdommen under de årlige epidemier i vintermånederne, har man designet et monoklonalt antistof, der kan binde sig til virussen og neutralisere den. Antistoffet kan gøre symptomerne ved sygdom mildere eller helt forhindre et udbrud. Symphogen A/S har i en årrække forsket i at producere et polyklonalt antistof mod RSV, og det antages, at dette antistof vil have bedre virkning end det eksisterende monoklonale pga. de polyklonale egenskaber. En af ulemperne ved de monoklonale antistoffer er nemlig, at de kun er specifikke mod et bestemt antigen, og dette kan være med til at selektere for resistente mutanter, der således med monoklonalt antistof vil undslippe behandling. Det forventes, at når dette produkt kommer på markedet, vil flere børn få mulighed for at modtage profylaktisk behandling, hvilket vil betyde, at langt færre spædbørn vil opleve alvorlige udbrud af RSV. Derved vil færre børn lide af de respiratoriske følgevirkninger efter en alvorlig RSV, og man vil desuden kunne mindske omkostningerne til senere hospitalsindlæggelser.
Et område hvor antistoffer som lægemidler er i kraftig udvikling, er kræftforskning. Der er her udviklet flere monoklonale antistoffer, som har vist god effekt. Antistofferne binder sig til forskellige overfladeproteiner, der enten er specifikke for kræftceller eller udtrykt i særlig høj grad i kræftceller, og de kan derfor lokalisere kræftcellerne og aktivere immunforsvaret til at dræbe dem. Andre af de monoklonale antistoffer virker ved at blokere bindingssteder for forskellige vækstinducerende molekyler. Derved kan kræftcellen ikke vokse lige så hurtigt, som den ellers ville have gjort. Der findes også antistoffer, der har bundet gift eller enzymer til deres Fc-region, som så leveres specifikt til kræftceller. Det uheldige ved kræftceller er, at de muterer. Hvis de molekyler, som antistofferne genkender (antigenerne), muterer, så mister antistofferne deres virkning, og man skal udvikle nye antistoffer specifikke for mutanten, der samtidig kan variere fra patient til patient.
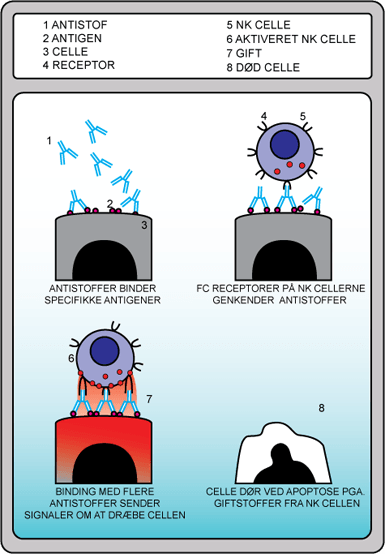
Figur 15. Figuren viser, hvordan antistofferne finder og binder den specifikke celle, der fx kunne være en kræftcelle. På den måde kan immunforsvaret angribe kræftcellen.
Figur 15 viser hvordan binding af antistoffer til en celle kan medføre, at denne dør. Binding af antistofferne tiltrækker Natural Killer celler (NK-celler) som indeholder cellegifte pakket i granula. Disse giftstoffer frigives ved binding af NK-cellen til antistoffernes Fc-del. Antistofferne tydeliggør på den måde cancercellerne for immunforsvaret, der herefter angriber cancerceller på samme måde, som var den en virus- eller bakterieinfektion.
TNF-alfa, eller tumor necrotic factor alpha, er et inflammatorisk cytokin. Det vil sige, at det er et molekyle, der fremmer inflammation og betændelse. Det bliver udskilt af bl.a. aktiverede makrofager, hvis de ”opfanger”, der er fare på færde, fx hvis de kommer i kontakt med en bakterie eller et viruspartikel. Det er fx cytokinernes skyld, at man får feber, når man bliver inficeret med en virus eller en bakterie.
Hvis det derimod er en autoimmun sygdom, der ligger til grund for udskillelsen af TNF-alfa og andre cytokiner, så kan immunforsvaret finde på at angribe kroppens egne og raske celler. Det er fx tilfældet i leddegigt, psoriasis og mutipel sclerose, der alle er autoimmunesygdomme. Det er i disse tilfælde derfor en fordel at begrænse mængden af inflammatoriske cytokiner. Det gør man fx. ved at producere antistoffer imod TNF-alfa. Antistofferne indfanger og neutraliserer TNF-alfa, hvorved den inflammatoriske reaktion fra den autoimmune sygdom begrænses. Disse antistoffer kaldes Anti-TNF-alfa antistoffer og er blevet en fast behandlingsmetode af leddegigt og andre autoimmunesygdomme.