Massespektrometri er en metode, der bestemmer massen af atomer og molekyler. Det er en meget anvendelig metode, som blandt andet kan bruges til at bestemme massen af organiske forbindelser, som er alt for små, til at vi kan veje dem med en vægt. Det kan f.eks. være kulhydrater, lipider, proteiner og DNA. Med avancerede former for massespektrometri kan forskere endda bestemme rækkefølgen af aminosyrer i et protein – sagt med andre ord, er det muligt at identificere proteinsekvenser med massespektrometri.
Teknikken bag
Det grundlæggende princip bag massespektrometri er, at en prøve med molekyler sendes igennem et massespektrometer, hvor den bliver udsat for et magnetfelt. Magnetfeltet får molekylerne til at accelerere. Hvor hurtigt molekylerne accelererer, afhænger af hvor tunge de er. Sammenhængen mellem kraft, acceleration og masse hedder Newtons 2. lov. Den siger, at kraften (F) er lig med massen (m) ganget med accelerationen (a).
Faktaboks
Sammenhængen mellem kraft (F), masse (m) og acceleration (a) kan beskrives med Newtons 2. lov. Den kraft, som en genstand bliver påvirket med, er lig med genstandens masse ganget med dens accelerationen.
Newtons 2. lov
![]()
Før magnetfeltet kan påvirke molekylerne i prøven, er de nødt til at have en ladning. Hvis molekylerne ikke har en ladning, vil de bare flyve direkte igennem magnetfeltet uden at blive påvirkede. Det nytter ikke noget, for magnetfeltets påvirkning er absolut nødvendig for at kunne bestemme massen af molekylerne. Molekyler er normalvis ikke ladede, fordi de har det samme antal elektroner som protoner. Hvis molekylerne skal blive ladede, er de nødt til at have et ulige antal elektroner og protoner. Det kan opnås, ved at molekylerne mister en elektron. Den proces kaldes også ionisering, fordi molekylerne bliver til ioner.
Ionisering
Der findes forskellige metoder til at ionisere molekylerne. Molekylerne kan f.eks. blive ioniserede ved at bombardere dem med elektroner. Når elektronstrålen rammer en elektron i molekylerne, kan den skubbe elektronen af. Hvis molekylerne mister én elektron, bliver de ioniserede og får ladningen +1. De ladede molekyler kan nu blive påvirket af magnetfeltet.
Når de ioniserede molekyler passerer gennem magnetfeltet, vil de blive afbøjede. På figur 1 kan du se en tegning af molekylernes vej igennem et massespektrometer. Molekylernes afbøjning afhænger af deres masse. Hvis molekylerne er lette, vil de accelerere meget, og så vil deres vej gennem massespektrometeret blive meget afbøjet. Hvis molekylerne er tunge, vil de kun accelerere lidt, og så vil de ikke blive særlig meget afbøjede. Det letteste molekyle på figur 1 er den gule, som afbøjer mest, mens det tungeste molekyle er den røde, som afbøjer mindst.
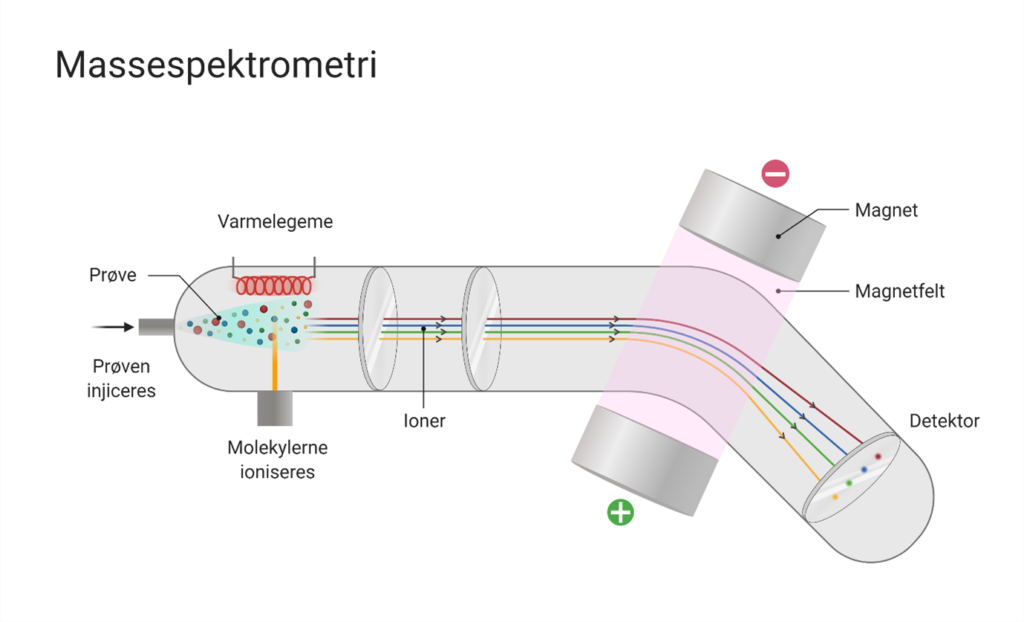
Alle de afbøjede molekyler bliver til sidst målt af en detektor, som måler deres acceleration. Når acceleration (a) er målt, kan Newtons 2. lov bruges til at bestemme massen (m) af molekylerne – se igen formlen for Newtons 2. lov. Kraften (F) fra magnetfeltet er en kendt størrelse, for forskeren indstiller selv magnetfeltets kraft på massespektrometeret inden forsøget.
Et eksempel på anvendelse af massespektrometri
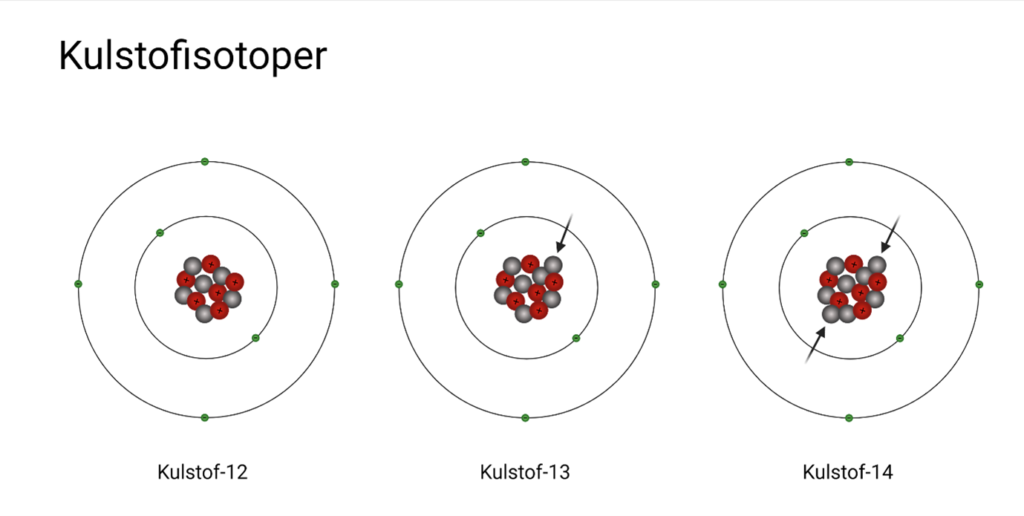
Massespektrometri kan bruges til mange forskellige formål. Metoden kan for eksempel bruges til at bestemme mængden af forskellige isotoper i en prøve. Isotoper er atomer, som har lige mange protoner, men et forskelligt antal neutroner. Antallet af neutroner i et atom har indflydelse på, hvor meget det vejer. Vi kan bruge kulstof, der har 6 protoner, som et eksempel. Kulstof-12 er den hyppigst forekommende kulstofisotop på jorden, men der findes også andre kulstofisotoper. For eksempel kulstof-13, der udgør omkring 1% af jordens kulstof, og kulstof-14 som findes i meget små mængder. Af de tre kulstofisotoper er kulstof-12 den letteste, fordi den har 6 neutroner, og kulstof-14 er den tungeste, fordi den har 8 neutroner. På figur 2 kan du se en tegning af de tre kulstofisotoper.
Kulstof-14-datering
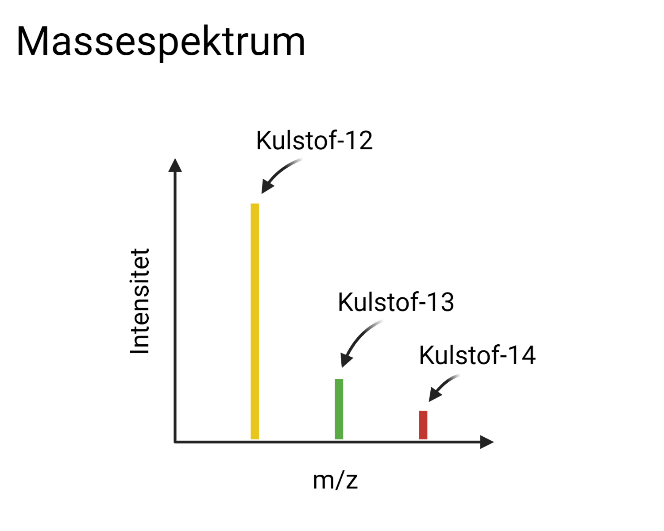
I en prøve med en blanding af de tre kulstofisotoper vil kulstof-12 accelerere mest, og kulstof-14 accelerere mindst, når den sendes igennem et massespektrometer. Når isotoperne rammer detektoren, kan Newtons 2. lov bruges til at bestemme deres masse ud fra deres acceleration. Derudover er det muligt at måle, hvor mange isotoper der er af hver slags. Det kan forskere bruge til at bestemme forholdet mellem de forskellige isotoper. Forholdet mellem kulstof-14 og kulstof-12, ![]() , kan forskerne for eksempel bruge til at bestemme, hvor gammelt et organisk materiale er. Det kaldes kulstof-14-datering. Metoden bliver brugt af arkæologer og forskere til blandt andet at bestemme alderen af menneskeknogler og døde planter, som de finder. På figur 3 kan du se et eksempel på et massespektrum for de tre kulstofisotoper.
, kan forskerne for eksempel bruge til at bestemme, hvor gammelt et organisk materiale er. Det kaldes kulstof-14-datering. Metoden bliver brugt af arkæologer og forskere til blandt andet at bestemme alderen af menneskeknogler og døde planter, som de finder. På figur 3 kan du se et eksempel på et massespektrum for de tre kulstofisotoper.
Proteinsekventering med massespektrometri
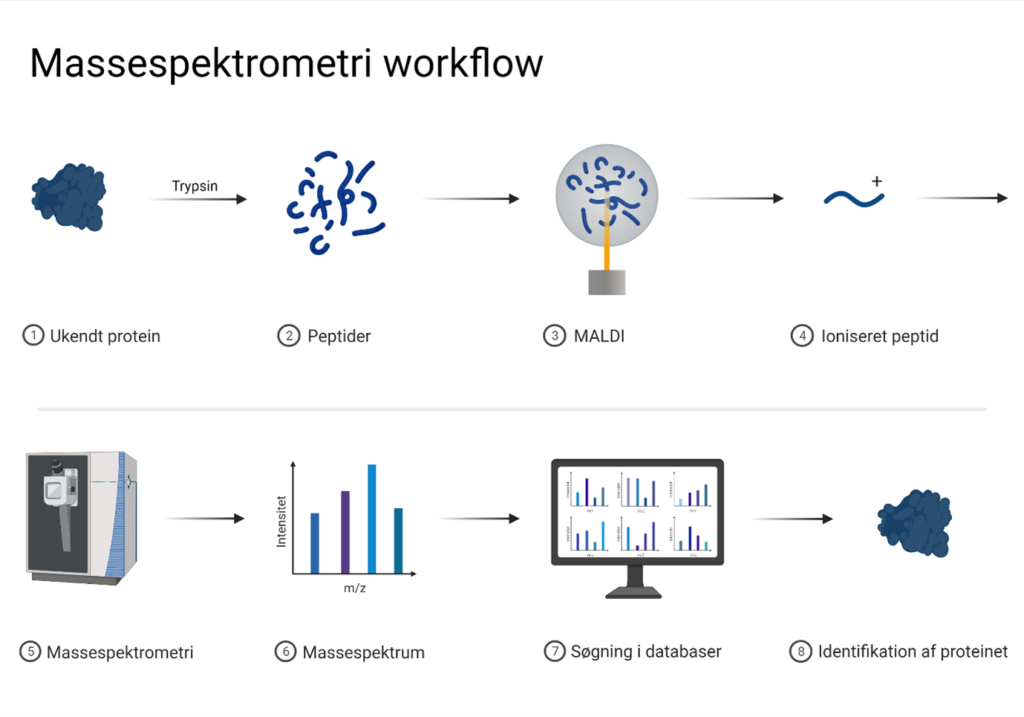
Massespektrometri kan bruges til at bestemme rækkefølgen af aminosyrer i et protein, kaldet proteinsekvensen. På figur 4 kan du se, hvordan man bestemmer en proteinsekvens med massespektrometri.
Proteiner fragmenteres til peptider
Før proteinet kan indsættes i massespektrometeret, skal det klippes i mindre stykker. Det gøres ofte med trypsin, som er et enzym, der klipper proteiner over. De små proteinstykker kaldes peptider, og de kan indsættes i massespektrometeret. Massespektrometeret laver et massespektrum for hvert peptid. Dét massespektrum sammenligner forskerne med massespektra fra en kæmpestor database for at finde et match, og på den måde regne ud hvordan peptidet er opbygget.
Massespektrum database
På figur 4 kan du se et eksempel på et massespektrum i trin 6, som bruges til at søge i en database i trin 7. Den store database består af massespektra, som en computer har lavet ud fra en genom-database. Computeren har taget alle DNA-sekvenserne i genom-databasen og omdannet dem til proteinsekvenser ved hjælp af proteinsyntesen også kaldet det centrale dogme. Derefter har computeren regnet ud, hvordan massespektrummet for hvert peptid i proteinerne vil se ud. Alle disse potentielle massespektra er samlet i en database, som forskerne kan søge i. Når forskerne har fundet et match mellem deres peptids massespektrum og et massespektrum fra databasen, kan de identificere sammensætningen af aminosyrer i deres peptid. Det matchende massespektrum fra databasen har en computer lavet ud fra et helt bestemt peptid.
Aminosyrerne i forskernes eget peptid, må være de samme, og det er derfor, at forskerne kan identificere dem. Når forskerne har gjort det for ét peptid, skal de også gøre det for alle de andre peptider i proteinet. Husk på, at de startede med at klippe proteinet i mindre stykker for at kunne indsætte det i massespektrometeret. Når forskerne har identificeret aminosyrerne i alle peptiderne, kan de samle alle puslespilsbrikkerne og bestemme hele proteinsekvensen.
Ionisering
En meget vigtig del af massespektrometri er at ionisere molekylerne, så de kan påvirkes af magnetfeltet. For at kunne bestemme en proteinsekvens med massespektrometri skal proteinet ioniseres, uden det bliver fuldstændig ødelagt. Hvis proteinet bliver ødelagt og splittet til aminosyrer under ioniseringen, bliver aminosyrerne i alle peptiderne målt i tilfældig rækkefølge. Så kan proteinsekvensen ikke identificeres. Forskere har udviklet forskellige metoder, som kan ionisere proteinerne på en skånsom måde. En af disse metoder hedder MALDI, som står for Matrix-Assisted Laser Desorption/Ionisation. Med MALDI bliver peptiderne lagt ind i en form, som kan absorbere lys. Når en laser rammer formen, bliver peptiderne ioniserede og slipper fri af formen. På figur 4 kan du se hele workflowet for, hvordan en proteinsekvens identificeres med massespektrometri.
Alle figurer er lavet med Biorender.com
« Back to Glossary Index
